«La celiaquía no es una intolerancia alimentaria, sino que es una enfermedad autoinmune, es decir, una situación en la que el propio sistema defensivo del organismo, en este tipo de casos, ataca por error a la mucosa del intestino delgado», subraya el Dr. José Carlos Marín Gabriel.
«El detonante de la autoagresión es el gluten, una proteína compuesta principalmente por gliadina y glutenina presente en cereales como el trigo, la cebada, el centeno o la espelta», señala el especialista en endoscopia digestiva del Hospital Universitario 12 de Octubre de Madrid.
Para entenderlo con una idea sencilla, imaginemos que el interior del intestino delgado es una alfombra de terciopelo, con millones y millones de pequeñas vellosidades que absorben los nutrientes.
«En una persona celíaca que consume gluten, su sistema inmunitario aplastará esas vellosidades hasta dejar la superficie intestinal lisa como un suelo de mármol, donde los nutrientes no podrán absorberse correctamente», explica el también director científico del Instituto Clínico del Aparato Digestivo (ICAdig).
Dr. Marín Gabriel, ¿por qué ahora parece que hay muchas más personas con celiaquía que en el pasado?
La enfermedad celíaca afecta a una o dos personas de cada cien en países donde el trigo es un alimento básico. Se diagnostica algo más en mujeres, pero no es exclusiva de ningún sexo ni de ninguna edad. De hecho, hasta un 20 % de los nuevos diagnósticos se realizan en personas mayores de sesenta y cinco años.
A la vez, existe un matiz muy importante a tener en cuenta: para desarrollar la enfermedad se necesita una predisposición genética concreta, los genes HLA-DQ2 ó HLA-DQ8 que están presentes en alrededor de un 30–40 % de la población general.
Sin embargo, aunque tengas esa predisposición genética no significa que vayas a ser celíac@, puesto que sólo un 1–2 % de quienes sean portadores acabarán desarrollando la enfermedad. Hace falta algo más, probablemente factores ambientales que todavía estamos terminando de entender.
¿Aumenta la incidencia de la enfermedad o se diagnostica con mayor eficacia?
Muy probablemente suceden ambas cosas. Por un lado, tenemos herramientas diagnósticas muchísimo mejores que hace treinta años.
En el análisis de sangre de referencia, los anticuerpos antitransglutaminasa tisular se empezaron a utilizar de forma generalizada a finales de los años noventa. Antes de eso, muchos casos sencillamente no se detectaban.
Pero también hay un aumento real. Valga un ejemplo: algún estudio ha analizado muestras de sangre conservadas de soldados estadounidenses de los años cincuenta y las han comparado con muestras actuales, y la prevalencia de anticuerpos celíacos se ha multiplicado.
Por tanto, algo ha cambiado en el entorno, no sólo en nuestra capacidad de diagnosticar.
Se barajan factores como cambios en la composición de los trigos modernos, alteraciones de la microbiota intestinal por el uso de antibióticos, o lo que se conoce como «hipótesis de la higiene», que sugiere que vivir en ambientes demasiado limpios puede desregular el sistema inmunitario (tema comentado en la entrevista sobre colitis ulcerosa),
De hecho, desde principios de los años 90, en las publicaciones médicas se popularizó la metáfora del «iceberg celíaco«, que hacía evidente la preocupación de los profesionales por la existencia de pacientes con la enfermedad que podrían estar sin diagnosticar.
Los casos diagnosticados, que sería la parte del iceberg que sobresale del agua, son una fracción del total. Debajo, sumergida, queda una proporción mucho mayor de personas que tienen la enfermedad, pero no lo saben.
Se calcula que, en la mayoría de los países, más del 50 % de las personas con celiaquía están sin diagnosticar. Y esas personas no diagnosticadas tienen más riesgo de complicaciones a largo plazo.
Doctor Marín, llama mucho la atención el infradiagnóstico de la celiaquía, ¿cómo se manifiesta la enfermedad en la edad adulta?
La enfermedad celíaca es una de las patologías que calificamos de «simuladora», ya que puede presentarse de muy diversas formas. Esto es así, en especial en los adultos.
Las manifestaciones clásicas de diarrea crónica y pérdida de peso son, de hecho, la forma menos frecuente de presentación. Hoy sabemos que en los adultos menos de la mitad debutan con síntomas digestivos típicos.
Muchos consultan por una anemia por pérdida de hierro que no se corrige con suplementos, por osteoporosis precoz, cansancio persistente, elevación inexplicable de las transaminasas del hígado, incluso por problemas de fertilidad.
También, hay manifestaciones neurológicas, aunque suelen ser raras. Entre estas, la más frecuente sería la neuropatía periférica, donde aparece dolor, hormigueo y entumecimiento muy molesto en manos y pies.
Pueden aparecer alteraciones de la marcha por problemas de coordinación y daño en el cerebelo (lo que denominamos ataxia), así como cefaleas recurrentes o migrañas, que afectan casi a una cuarta parte de l@s celíac@s.
Además, los síndromes de fatiga crónica y “niebla mental” se han descrito como formas raras de presentación de la enfermedad.
Y entre otras formas relativamente frecuentes de presentación está la afectación en la piel en forma de dermatitis herpetiforme, que es una erupción con vesículas muy características que suele afectar a codos y rodillas.
Para que nos hagamos una idea, una persona de 45 años que acude al médico por llevar meses con fatiga y le encuentran una ferritina baja sin una causa aparente podría perfectamente ser celíaca. O una mujer de 50 años a la que diagnosticaron osteoporosis y nadie piensa en pedir un análisis de anticuerpos.
El retraso diagnóstico medio en adultos ronda los nueve años en muchos estudios. Eso quiere decir que hay personas conviviendo con una enfermedad tratable durante casi una década sin saberlo, exponiéndose a complicaciones que pueden evitarse.
Doctor, hablemos de mitos o bulos en la celiaquía: un buen número de personas piensan que la ausencia de síntomas digestivos evidentes descartan el padecimiento de la enfermedad, ¿es cierto?
La idea de que «si no tienes diarrea no eres celíaco» ha sido la principal causa de retraso diagnóstico durante décadas. Como hemos comentado, la enfermedad puede presentarse exclusivamente con manifestaciones extraintestinales, incluso ser completamente silente desde el punto de vista clínico.
Las guías de práctica clínica actuales recomiendan buscar activamente la enfermedad en lo que llamamos «grupos de riesgo»:
- Familiares de primer grado de pacientes celíacos, donde la prevalencia puede llegar al diez por ciento.
- Personas con diabetes tipo 1.
- Pacientes con tiroiditis autoinmune.
- Personas con anemia ferropénica sin causa clara.
- Pacientes con osteoporosis precoz, o con elevación inexplicable de enzimas hepáticas.
Y volvemos al asunto del iceberg. Un médic@ que sólo busca celiaquía cuando hay diarrea está viendo únicamente una pequeña fracción del problema.
Las guías nos dicen claramente que debemos tener un umbral bajo para solicitar los anticuerpos. Un simple análisis de sangre con anticuerpos antitransglutaminasa IgA y determinación de IgA total suele ser suficiente para el cribado inicial, y es una prueba barata y accesible.

Doctor, muchos pacientes informan a sus médic@s de que sufren hinchazón abdominal, gases y episodios de diarrea durante años y años, y la respuesta más habitual que reciben les indica que padecen colon irritable o sobrecrecimiento bacteriano… ¿Es posible que detrás se esconda la celiaquía?
No sólo es posible, sino que es más frecuente de lo que pensamos. La enfermedad celíaca y el síndrome del intestino irritable comparten síntomas que se solapan enormemente: distensión abdominal, dolor, alteración del hábito intestinal y gases.
Un paciente con celiaquía no diagnosticada puede pasar años etiquetado como colon irritable porque nadie le ha pedido los anticuerpos.
Por eso, las Guías de Práctica Clínica recomiendan expresamente descartar la celiaquía en pacientes con síndrome del intestino irritable puesto que, en estos pacientes, la frecuencia de la enfermedad celíaca es mayor que la de la población general.
Con el sobrecrecimiento bacteriano ocurre algo parecido. Los síntomas de hinchazón y diarrea se atribuyen al SIBO, pero la propia celiaquía produce alteraciones en la motilidad intestinal y en el microbioma que pueden mimetizar o incluso inducir un sobrecrecimiento bacteriano en el intestino delgado.
La recomendación es que, ante un paciente con síntomas digestivos inespecíficos que no acaban de resolverse, antes de asumir que es funcional o que es SIBO, hay que descartar celiaquía. Es una de las causas tratables de malabsorción más frecuente, y no dar con el diagnóstico tiene consecuencias a largo plazo.
¿Y cómo se diagnostica la celiaquía en un adulto, puesto que no basta con un análisis de sangre y tampoco se practica una biopsia del tejido duodenal a todo el mundo?
El esquema estándar en adultos sigue siendo una estrategia en dos pasos: primero serología, después biopsia confirmatoria.
El análisis de sangre inicial es la antitransglutaminasa IgA, que debe solicitarse siempre junto con una IgA total, porque si el paciente tiene un déficit de IgA, que es relativamente frecuente en la población, el resultado de la antitransglutaminasa puede ser falsamente negativo.
Si la antitransglutaminasa sale positiva, el siguiente paso es una endoscopia con biopsias de duodeno:
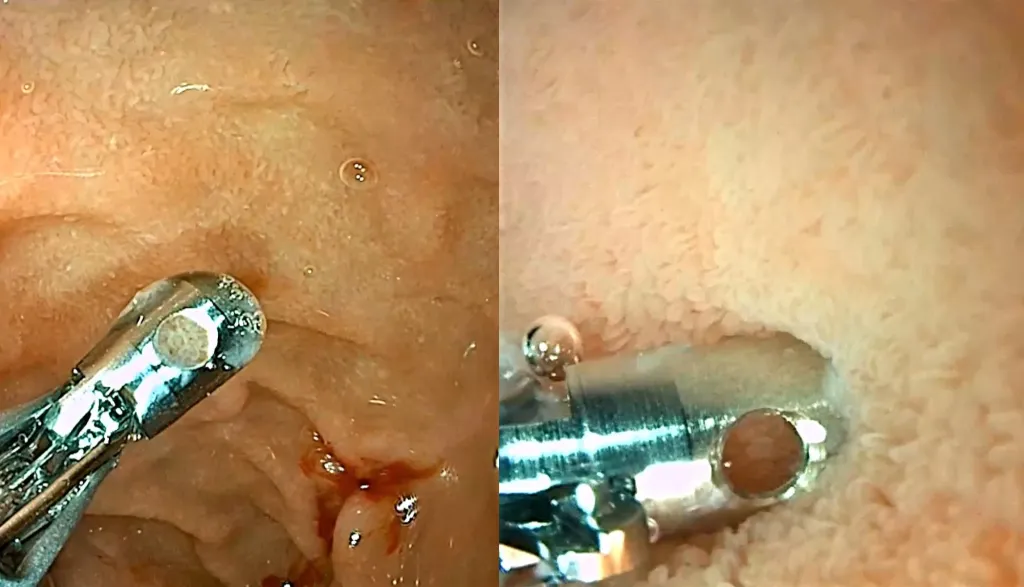
Se recomienda tomar una o dos muestras de la parte del duodeno más cercana al estómago, el bulbo duodenal, y al menos cuatro del duodeno distal. Esto es así porque las lesiones pueden ser parcheadas y, si no se toman suficientes muestras, se puede pasar por alto el diagnóstico.
Sin embargo, no siempre es tan fácil el diagnóstico. Hay una situación que llamamos enfermedad celíaca seronegativa: pacientes que tienen la enfermedad, pero con anticuerpos normales en sangre.
En estos casos, cuando la sospecha es alta, se debe realizar la endoscopia con biopsias duodenales independientemente del resultado de la serología.
¿Y qué situaciones generan esa alta sospecha?
Por ejemplo, un familiar de primer grado con celiaquía confirmada, una anemia ferropénica que no responde a hierro oral, una dermatitis herpetiforme, transaminasas elevadas sin causa aparente, o esos síntomas digestivos crónicos que no encajan del todo en un cuadro funcional.
Entonces, doctor Marín, ¿dónde encaja la prueba genética en el proceso del diagnóstico de la celiaquía?
Empecemos por el principio. Nuestros genes tienen “los planos” para fabricar las “piezas” que son las proteínas de nuestras células, ¿verdad?
Pues bien, en una región del cromosoma 6, están los genes HLA, con las instrucciones para fabricar las proteínas del HLA, que es el acrónimo en inglés de “Antígeno Leucocitario Humano”.
Estas proteínas se colocan en la superficie de algunas células del sistema inmunológico y funcionan como un escaparate. Enseñan pequeños fragmentos de proteínas a otras células de defensa para que decidan si hay que reaccionar. Son algo así como los agentes infiltrados que les pasan las pruebas a la policía y que puedan detener a los criminales.
En la celiaquía, tus genes “fabrican” unos tipos de HLA llamados DQ2 y/o DQ8. Y con estas versiones del HLA una parte del gluten llamada gliadina encaja especialmente bien, como una llave en su cerradura.
Esa unión, en determinadas personas, facilita que se activen otras células de defensa y se ponga en marcha una respuesta inflamatoria que acaba dañando el intestino. Por eso, los médicos buscamos esos dos tipos de HLA cuando sospechamos una celiaquía.
¡Pero atención!… Si tu tipaje HLA es DQ2 o DQ8 no implica necesariamente que padezcas una enfermedad celíaca. Ambos están presentes en el 30-40 % de la población general sin ser celíacos. El DQ2 y el DQ8 son condición necesaria pero no suficiente.
Por otra parte, tienen un valor extraordinario para descartarla. Si un paciente en el que sospechamos la enfermedad no tiene DQ2 y DQ8 positivos, la probabilidad de que sea celíac@ es prácticamente nula.
Este análisis del HLA es especialmente útil en dos escenarios: cuando hay discrepancias entre la serología y la biopsia (un HLA no compatible descarta el diagnóstico) y cuando el paciente ya ha empezado una dieta sin gluten por su cuenta antes de hacerse las pruebas.
En este último caso, los antitransglutaminasa pueden haberse normalizado y la biopsia puede haber mejorado, pero el HLA no habrá cambiado ni cambiará.
Si es compatible, se puede plantear una provocación con gluten para intentar llegar al diagnóstico; si es negativo, podemos y debemos buscar otra causa que explique los síntomas.
En resumen, el diagnóstico de la celiaquía del adulto es como un puzle de tres piezas: serología, biopsia y genética. No siempre se necesitan las tres, pero hay que saber cuándo recurrir a cada una.
Y aquí hay dos mensajes importantes: un análisis de sangre negativo no descarta la enfermedad si la sospecha clínica es alta. En esos casos, hay que dar paso a la biopsia. Y un HLA compatible, DQ2 ó DQ8, no permite diagnosticar la enfermedad por sí mismo.

Dr. Marín Gabriel, es muy conocido a nivel popular que el tratamiento de la enfermedad celíaca consiste básicamente en eliminar el gluten de la dieta; sin embargo, comer alimentos sin gluten se ha convertido en una tendencia o moda social… ¿Retirar el gluten de nuestra dieta reporta algún beneficio a las personas que no padecen la enfermedad?
Este asunto es muy relevante porque aquí la desinformación está muy extendida. ¿Qué datos tenemos respecto a esto? Parece que la cantidad de personas que se autodiagnostican de «sensibilidad al gluten» oscila entre un 6-13 % de la población total.
Pero, cuando esos pacientes se someten a estudios rigurosos, doble ciego y controlados con placebo, en los que se practican pruebas de provocación con gluten, sólo una minoría resultan ser celíac@s.
Un estudio, publicado recientemente en una de las revistas más prestigiosas de nuestra especialidad del grupo Lancet, demostró que el efecto de las expectativas, lo que llamamos «efecto nocebo» (llego a sentirme mal porque creo que voy a estar mal), juega un papel muy relevante en la percepción de síntomas.
Esto no quiere decir que la sensibilidad al trigo no celíaca no exista. Existe, pero es mucho menos frecuente de lo que se cree y su diagnóstico es complejo.
Además, hay que tener en cuenta que los cereales con gluten contienen también otros componentes como los FODMAP (hidratos de carbono fermentables) y los inhibidores de la amilasa-tripsina, que podrían explicar los síntomas en muchos casos, sin que el gluten siempre sea el culpable.
En cuanto a retirar el gluten sin supervisión médica, hay que insistir en que genera dos problemas.
Por un lado, puede enmascarar una enfermedad celíaca real: si dejas de comer gluten y después te haces la prueba de los anticuerpos, los resultados pueden salir negativos, aunque seas celíaco, porque la respuesta inmunitaria necesita la exposición al gluten para ser detectable. Estarías tapando un diagnóstico importante.
Por otro lado, algunos productos procesados «sin gluten» son más ricos en azúcares y grasas saturadas para compensar el sabor; y una dieta sin gluten no supervisada puede ser deficiente en fibra, hierro, vitaminas del grupo B y ácido fólico.
En resumen, cuando un paciente sospecha un problema con el gluten, lo primero que debe hacer es ir al médic@ y hacerse las pruebas antes de retirarlo de la dieta por tu cuenta.
Doctor, existe la idea, viralizada en las redes sociales, de que ciertos productos o suplementos alimenticios permiten a las personas celíacas «relajarse un poco» con la dieta estricta. En este sentido, ¿funcionan los probióticos y las enzimas que degradan el gluten?
Vivir sin gluten en una cultura mediterránea donde el pan, la pasta y la cerveza son los verdaderos protagonistas puede ser realmente complicado. Y las expectativas con esta oferta de productos resulta ilusionante y atractivo. Pero hay que ser muy honestos y rigurosos desde el punto de vista científico.
Respecto a las enzimas digestivas, que supuestamente degradan el gluten, como la latiglutenasa o la AN-PEP, los resultados de los ensayos clínicos han sido decepcionantes.
Latiglutenasa, por ejemplo, ha pasado por el ensayo clínico más grande realizado en enfermedad celíaca y no logró demostrar superioridad frente a placebo en su objetivo principal.
Estas enzimas pueden degradar pequeñas cantidades de gluten residual, pero no son capaces de proteger frente a una exposición significativa. Por desgracia, no son un «seguro» para comer una ración de macarrones con salsa de boloñesa.
En cuanto a los probióticos, hay un interés creciente porque sabemos que la microbiota intestinal de los pacientes celíacos difiere de la de las personas sanas, con una menor diversidad bacteriana, especialmente bífidus (Bifidobacterium).
Pero esto podría ser consecuencia de la enfermedad y no parte del problema original.
Algunos estudios preliminares sugieren que ciertos probióticos podrían, de forma marginal, mejorar algunos síntomas. Sin embargo, no tenemos aún estudios de calidad suficiente para confirmar su supuesto efecto beneficioso.
De hecho, las guías de práctica clínica actuales concluyen que no hay evidencia suficiente para recomendar el uso de probióticos como tratamiento complementario en la enfermedad celíaca.
En la mayoría de estudios se incluyen pocos pacientes, con seguimientos cortos y desenlaces que no son relevantes para los celíacos (por ejemplo, cambios en el microbioma en lugar de calidad de vida).
Para terminar de complicarlo, algunos estudios incluso han encontrado problemas de seguridad, con contaminación por gluten en productos probióticos que estaban etiquetados como “sin gluten”.
Lo que sí funciona es una dieta sin gluten estricta y bien planificada, con asesoramiento personalizado en la consulta de un o una dietista-nutricionista experimentad@ en celiaquía.
Me temo que no hay atajos con las terapias complementarias disponibles actualmente. Por ahora, ningún suplemento, enzima o probiótico, sustituye a la dieta sin gluten estricta. Desconfíe de cualquier producto que prometa «neutralizar» el gluten de una comida.
Dr. Marín Gabriel, ¿qué avances diagnósticos destacaría para l@s pacientes celíac@s?
En niñas y niños, las guías europeas ya permiten desde 2012 un diagnóstico sin biopsia cuando los anticuerpos antitransglutaminasa superan diez veces el límite superior de la normalidad. Esto ha simplificado mucho el diagnóstico en pediatría.
La pregunta del millón es si podemos trasladar eso a los adultos.
Un estudio multicéntrico, publicado en Gastroenterology hace un par de años, valoró la capacidad predictiva de los anticuerpos antitransglutaminasa IgA muy elevados en adultos para predecir la presencia de atrofia vellositaria, y los resultados fueron prometedores.
De hecho, puede que en el futuro próximo veamos el diagnóstico sin biopsia en adultos seleccionados, aunque de momento la biopsia duodenal sigue siendo el estándar.
En todo caso, hay que ser prudentes porque en adultos el diagnóstico diferencial es más amplio. Hay otras enfermedades que pueden dar imágenes similares en la biopsia, como los efectos de ciertos fármacos (antihipertensivo olmesartán, etc.), o el sobrecrecimiento bacteriano.
La biopsia, por tanto, sigue aportando información valiosa. Pero no me sorprendería que en los próximos años las guías europeas se revisen para permitir un diagnóstico sin biopsia en adultos con títulos muy altos de anticuerpos, como ya se hace en los niños.
Otro avance relevante es la detección repetida de péptidos inmunogénicos del gluten en orina o en heces, que pueden detectar la exposición al gluten (voluntaria o no), de forma más fina que los niveles de anticuerpos en sangre.
Esto permite monitorizar de forma objetiva si el paciente se está “saltando” la dieta sin gluten. Algo que hasta ahora dependía de lo que nos contaba en la consulta o de la determinación de anticuerpos en sangre, que pueden estar bajos, aunque exista daño intestinal.
Doctor, hablemos de los tratamientos futuros, puesto que tomar una dieta sin gluten de por vida debe resultar muy demandante. ¿La investigación muestra algún avance farmacológico cercano?
Después de veinte años de ensayos clínicos, todavía no hay ningún fármaco aprobado para la enfermedad celíaca, lo cual da idea de la complejidad del problema. Pero sí hay candidatos muy interesantes en fases tempranas de desarrollo.
Uno de los más avanzados es el TAK-227, también conocido como ZED-1227, un inhibidor de la transglutaminasa tisular, que es la enzima clave que potencia la respuesta inmunitaria al gluten.
Un ensayo fase 2 publicado en el New England Journal of Medicine en 2021 mostró que este fármaco atenuaba el daño intestinal en pacientes celíacos sometidos a una provocación diaria con gluten.
Actualmente, está en marcha otro ensayo en pacientes con síntomas persistentes a pesar de la dieta sin gluten.
Otra línea de investigación interesante es la de las terapias que buscan reeducar al sistema inmunitario para que tolere el gluten, lo que llamamos «inducción de tolerancia».
KAN-101, por ejemplo, es un péptido de gluten conjugado que se dirige al hígado para generar una respuesta tolerogénica. Está en fases iniciales de desarrollo y aún es pronto para sacar conclusiones, pero el concepto es muy atractivo: si funcionase, sería como desactivar la alarma que el sistema inmunitario dispara cuando detecta el gluten.
Por supuesto, ninguno de estos fármacos va a estar disponible muy pronto. Los escenarios más realistas plantean que las primeras terapias aprobadas probablemente sean complementarias a la dieta sin gluten, no sustitutivas, y estarían dirigidas a pacientes que no responden adecuadamente o que tienen exposiciones involuntarias frecuentes.
El sueño de poder comer gluten sin consecuencias para la salud de un celíaco está todavía lejos, pero los investigadores avanzan con ese objetivo en mente.

¿Y qué papel jugará la inteligencia artificial en la enfermedad celíaca, protagonista o secundario?
La IA está empezando a tener aplicaciones muy interesantes, y en la endoscopia, que no deja de ser una técnica de imagen, es uno de los campos donde más está avanzando.
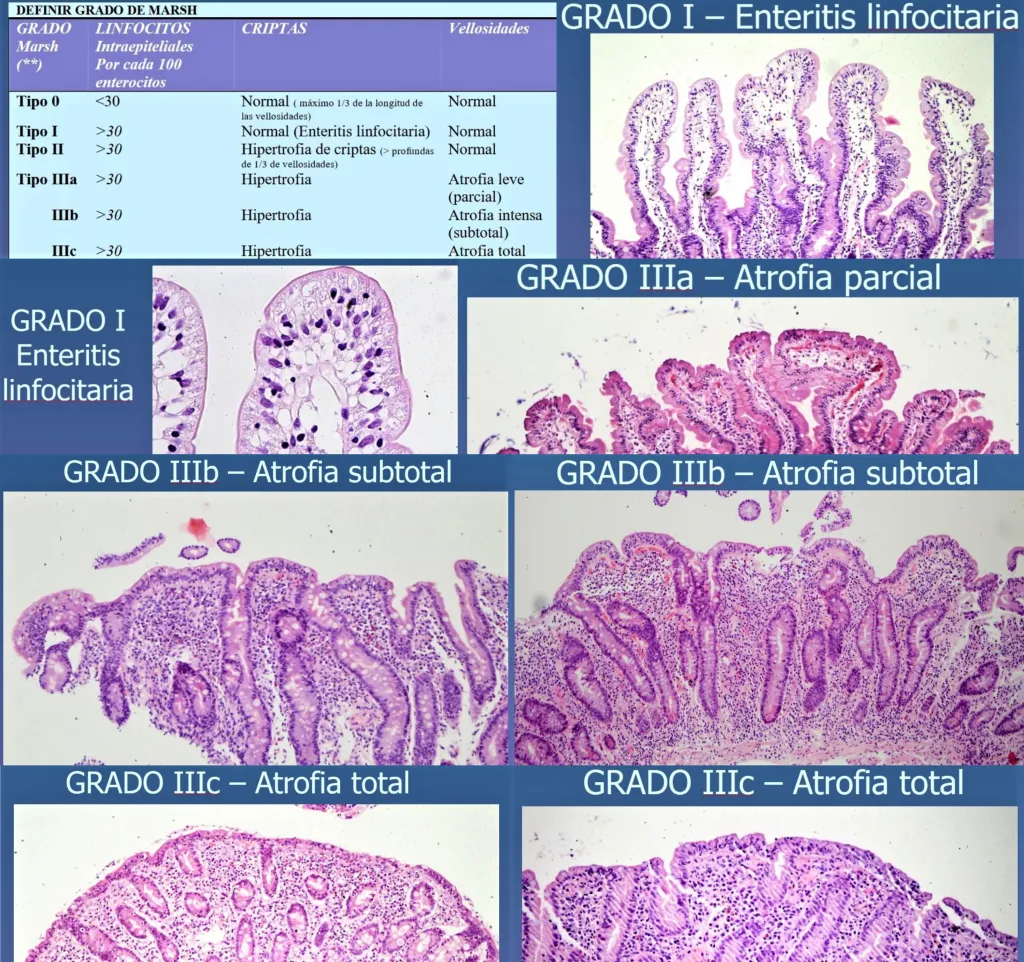
Se han desarrollado sistemas que, durante una gastroscopia, pueden analizar en tiempo real el aspecto de la mucosa duodenal y detectar signos sutiles de atrofia vellositaria que podrían pasar desapercibidos a simple vista.
Además, se están desarrollando puntuaciones cuantitativas automatizadas que analizan la relación entre la altura de las vellosidades y la profundidad de las criptas intestinales, lo que podría estandarizar la evaluación de la respuesta a la dieta sin gluten.
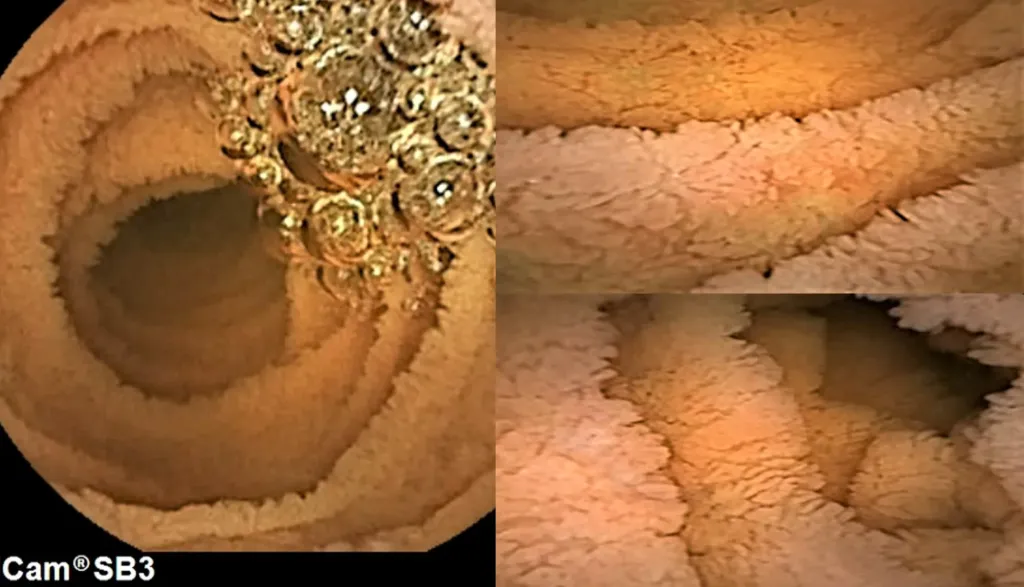
La cápsula endoscópica con análisis asistido por inteligencia artificial también ofrece posibilidades para documentar la curación de la mucosa de forma menos invasiva que una gastroscopia convencional.
De nuevo, la mayoría de estas aplicaciones están en fase de desarrollo o de validación. Todavía no se han integrado de forma rutinaria en la práctica clínica diaria.
La IA es una herramienta prometedora que probablemente mejore nuestra precisión diagnóstica, pero aún hoy no sustituye al buen criterio médico ni una buena historia clínica. La tecnología nos ayuda, pero el centro del proceso debe seguir siendo la relación entre el médico y su paciente.

Una persona celíaca, diagnosticada y que ya tiene asignada una dieta sin gluten muy estricta, ¿qué más puede hacer para mejorar su bienestar y calidad de vida?
Lo primero y más importante es que la dieta sin gluten esté bien asesorada por un dietista-nutricionista con experiencia en enfermedad celíaca.
Esto no es un capricho… Los estudios muestran que l@s pacientes que reciben educación dietética especializada tienen mejor adherencia y calidad de vida. No basta con «quitar el pan y la pasta», porque el gluten se esconde en muchos productos procesados, salsas o embutidos.
También hay que tener en cuenta que la contaminación cruzada es real y relevante.
En casa conviene tener utensilios separados si convives con personas que comen gluten, sobre todo la tostadora, las tablas de cortar y los coladores.
Fuera de casa, advertir de la situación en el restaurante no es exageración ni manía, es una necesidad médica. Por fortuna, el mundo profesional de la hostelería está cada vez más concienciado en lo que respecta a esta enfermedad.
El seguimiento médico periódico también es fundamental.
La enfermedad celíaca no es de esas que se diagnostican y se olvidan. Las guías de buenas prácticas recomiendan controles regulares que incluyan serología, analítica nutricional completa y valoración de la densidad ósea, especialmente en los primeros años tras el diagnóstico.
Muchos adultos celíacos tienen déficit de hierro, vitamina D, calcio o ácido fólico al diagnóstico, y hay que monitorizar su recuperación.
Y algo que a veces se olvida: cuidar la salud emocional. Vivir con una restricción alimentaria crónica tiene un impacto psicológico real, especialmente en la vida social.
No hay que banalizar esa carga. Si el paciente lo necesita, es muy recomendable buscar apoyo en asociaciones de celíacos, incluso en profesionales de la salud mental.
Doctor Marín, ¿y qué señales de alarma nos advierte de una posible celiaquía?
Yo diría que hay que plantearse la posibilidad de celiaquía y consultar al médico en los siguientes casos:
- Diarrea crónica o alternancia entre diarrea y estreñimiento que no se explica por otras causas, especialmente si se acompaña de distensión abdominal persistente.
- Anemia por pérdida de hierro que no responde a la suplementación o que reaparece tras completar el tratamiento.
- Pérdida de peso no buscada ni explicada.
- Cansancio persistente que interfiere con la vida diaria y no mejora con descanso.
- Diagnóstico de osteoporosis o fracturas por fragilidad, sobre todo antes de los cincuenta y cinco años.
- Familiares de primer grado con enfermedad celíaca confirmada, aunque no se tenga ningún síntoma.
- Presencia de otras enfermedades autoinmunes, particularmente diabetes tipo 1 o tiroiditis autoinmune.
- Elevación inexplicable de las transaminasas hepáticas.
- Problemas reproductivos como infertilidad, abortos de repetición o retraso puberal.
- Aftas bucales recurrentes.
Por supuesto, no hace falta tener todos estos síntomas: a veces basta con uno solo. Y un análisis de anticuerpos antitransglutaminasa IgA, junto con una determinación de IgA total, es una prueba sencilla, no invasiva y muy accesible.
Lo esencial es que el médico piense en la posibilidad de una celiaquía oculta, porque no vamos a encontrar algo que no se busque intencionadamente, salvo casualidad o fortuna.
Para finalizar la entrevista, doctor Marín, ¿qué mensaje envía al conjunto de la población, padezca o no la celiaquía, con o sin diagnóstico?
Serían solo tres cosas: la primera es que la enfermedad celíaca es frecuente y se diagnostica menos de lo debido.
Cualquier adulto puede desarrollarla, independientemente de su edad, y muchas veces la cara visible no es la diarrea sino una anemia, una osteoporosis o un cansancio que no tiene explicación aparente. Si algo no encaja en tu salud, pregúntale a tu médico si podría ser celiaquía. Es una gran simuladora.
La segunda idea es que el diagnóstico cambia vidas. Personas que llevaban años arrastrando síntomas encuentran una mejoría espectacular con la dieta sin gluten.
Aún así, para que el diagnóstico sea fiable, es imprescindible hacerse las pruebas antes de retirar el gluten por cuenta propia. Si comienzas a practicar una dieta sin gluten antes de las pruebas pertinentes se dificulta el diagnóstico de la celiaquía.
Y la tercera: la ciencia sigue avanzando. Hoy, la dieta sin gluten sigue siendo el único tratamiento, pero hay investigaciones muy prometedoras con fármacos que en los próximos años podrían ofrecer una red de seguridad adicional a nuestros pacientes.
Mientras tanto, con un buen seguimiento médico, una alimentación bien planificada y apoyo adecuado, una persona celíaca puede llevar una vida absolutamente normal. No hay que resignarse ni dramatizar, sólo estar bien informado y actuar en consecuencia.
En la próxima Consulta de Aparato Digestivo preguntaremos al Dr. José Carlos Marín Gabriel sobre la gastrostomía, un procedimiento quirúrgico o endoscópico por el que se coloca una sonda de alimentación externa conectada al estómago, atravesando la pared abdominal.

